1.- Modelo de Dalton
Pre-conocimiento
¿Has oído alguna vez hablar del daltonismo? Seguro que sí.
Es un defecto de la visión que padecen algunas personas y que les hace confundir ciertos colores. Lo que una persona ve de color rojo, por ejemplo, un daltónico lo ve de color azul.
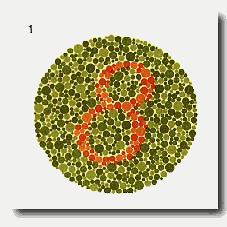 |
 |
 |
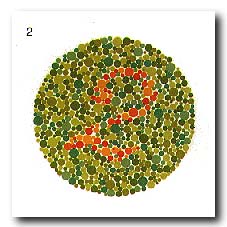
| Imagen de dominio público. Test de daltonismo. | ||
Mira la imagen de arriba a ver qué número ves... ¿Has visto un 825? ¿Sí? Pues entonces no eres daltónico. Pero si no es así... deberías hacerte pruebas para descubrirlo... puede que lo seas y aún no lo sepas.
Y... ¿qué tiene todo esto que ver con los átomos? Pues la verdad es que nada. Bueno, casi nada. El daltonismo se llama así en honor al primer protagonista de nuestra historia sobre los modelos atómicos: John Dalton.
A la edad de 26 años, Dalton le regaló a su madre una medias que él creía eran de color azul. Pero resulta que no, que eran rojas (un color nada apropiado para una mujer de la edad de la madre de Dalton). Entonces fue cuando empezó a investigar esa incapacidad suya para distinguir algunos colores y fue el primero en hacer una descripción científica de este defecto de la visión.
Lo que Dalton pretendía retomando la teoría atómica era explicar ciertas regularidades que se observaban en la forma en que unas sustancias reaccionaban con otras, en las reacciones químicas. Estas regularidades, conocidas como leyes ponderales de la química, eran bien conocidas y estaban bien documentadas en la época de Dalton (siglo XIX).
Pre-conocimiento
Algunas de las leyes ponderales, pero no las únicas, son las siguientes:
- Ley de conservación de la masa: Establece que en toda transformación química, permanece invariable la masa total del sistema, es decir, la masa total de las sustancias que reaccionan es exactamente igual a la masa total de las sustancias que se producen en la reacción.
- Ley de las proporciones constantes: Establece que cuando varios elementos se combinan entre sí para dar un determinado compuesto, lo hacen siempre en la misma proporción en masa.
Pues éstas leyes tan simples, y algunas más, conocidas como Leyes Poderales, eran las leyes que se utilizaban para estudiar los procesos químicos.
¿Nada más que esto se conocía?, ¿éstas eran todas las leyes de la Química?. Pues peor aún, todas estas leyes fueron obtenidas de forma experimental, y ni tan siquiera había una teoría sobre la materia que las explicara.
Si tienes curiosidad por conocer más cosas sobre estas Leyes Poderales, puedes utilizar el siguiente enlace:
Dalton sugirió que todas esas leyes de la Química se podrían explicar muy fácilmente si suponemos que la materia está formada por átomos. Imaginaba los átomos como esferas rígidas, indivisibles e indestructibles, de tal manera que los átomos de cada elemento químico eran todos iguales entre sí, pero diferentes a los de los demás elementos.
|
|
“La materia está compuesta de átomos de diferentes masas, que se combinan en proporciones sencillas para formar compuestos" John Dalton |
Actividad
Las hipótesis en las que Dalton basaba su modelo eran las siguientes:
|
|
- Los elementos están formados por partículas diminutas, e indivisibles llamadas átomos. Los átomos de un mismo elemento son todos iguales entre sí en masa, tamaño y en cualquier otra propiedad.
- Los compuestos químicos están formados por unas partículas, llamadas moléculas, todas iguales entre sí. Es decir, las moléculas se forman por la unión de varios átomos.
- En las reacciones químicas, los átomos ni se crean ni se destruyen, sólo cambia la manera en que están unidos. Las reacciones químicas son pues una redistribución de los átomos.