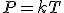4.3 Ley de Gay-Lussac
|
|
| Louis Joseph Gay-Lussac (1778-1850). Imagen de wikipedia |
Gay-Lussac estudió experimentalmente el comportamiento de los gases cuando se calentaba una masa fija de gas en un recipiente de volumen constante. Observó que al aumentar la temperatura, la presión también lo hacía de forma proporcional.
En la siguiente animación puedes observar y escuchar la explicación, de lo que ocurre cuando se calienta o enfría un gas que se encuentra en un recipiente de volumen constante.
| Animación de Jesús Peñas disponible en Averroes |
Si tomamos anotamos los valores de la presión a distintas temperaturas y los representamos gráficamente, obtenemos una línea recta, lo que indica que la presión es directamente proporcional a la temperatura en Kelvin, tal como se muestra en la figura siguiente.
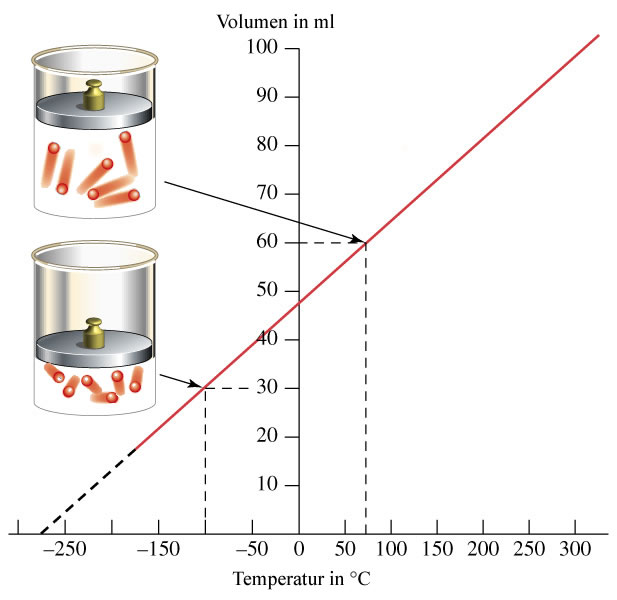 |
| Imagen de Rittmeister, Creative commons |
Esta ley se suele explicitar como P/T=cte o bien Pi/Ti=Pf/Tf
De la misma forma que antes, extrapolando la recta resultante en la zona de bajas temperaturas, se obtiene que la presión se anularía a -273ºC (0 K).
Actividad
Ley de Gay-Lussac:
A volumen constante, la presión ejercida por un gas es directamente proporcional a la temperatura en Kelvin.