La materia. Lenguaje químico: Fórmula empírica y molecular. Composición centesimal
|
|
|
Preparación Acceso a CFGS |
|
Química |
|
Contenidos
|
|
La materia. Lenguaje químico:Fórmula empírica y molecular. Composición centesimal |
|
 |
| Molécula de agua CC0 |
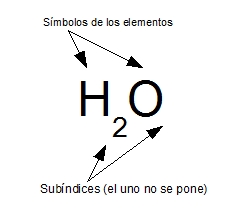 |
Sabes que el agua es una sustancia formada por moléculas cuya fórmula es H2O. Pero, ¿qué significado tiene dicha fórmula? Seguro que respondes a esta pregunta diciendo que el agua está formada por los elementos hidrógeno y oxígeno, y que en cada molécula de agua se unen dos átomos de hidrógeno a un átomo de oxígeno.
Pues exactamente esa es la información que podemos extraer de la fórmula de una sustancia molecular como el agua: es una expresión que indica los elementos químicos que forman una sustancia (que se representan mediante sus símbolos), y el número de átomos de esos elementos que hay en una molécula, (que se indican mediante subíndices que se escriben a la derecha del símbolo del elemento y que tienen que ser números enteros mayores que cero).
 |
| Cristal NaCl Dominio Público |
Pero como hemos visto en el tema anterior, no todas las sustancias están formadas por moléculas, en muchas sustancias sólidas millones de átomos están ordenados en el espacio formando redes o cristales. En los cristales no existen moléculas y la fórmula química indica la relación en la que se encuentran los átomos de los elemento en la red. Así, la fórmula del cloruro de sodio (NaCl) indica que en la red cristalina, por cada átomo de sodio hay un átomo de cloro.
En este tema vas a aprender a diferenciar entre fórmula empírica y fórmula molecular, a hallar dichas fórmulas a partir de datos experimentales obtenidos en los laboratorios, y a calcular la composición centesimal de un compuesto.
