7. Análisis de sustancias: espectroscopia y espectrometría
Uno de las grandes labores de un químico es la de enfrentarse a una muestra y poder conocer su composición.
Las técnicas espectroscópicas permiten el análisis de sustancias y la detección de las mismas en cantidades muy pequeñas de muestras.
 |
| Imagen de Poul la Cour & Jacob Appel en Wikipedia. CC0 |
Durante el siglo XX, gracias a los avances en el conocimiento de las radiaciones electromagnéticas, se diseñaron técnicas analíticas basadas en la interacción de la luz con la materia. Estas son las técnicas espectroscópicas, entre las que se encuentran: espectroscopía atómica, espectroscopía Raman, colorimetría, resonancia magnética nuclear (RMN), espectroscopía de absorción infrarroja (IR), además de la espectrometría de masas en la que se lleva a cabo un bombardeo de electrones (a diferencia de las anteriores, esta no se basa en la interacción luz-materia).
Se utiliza el espectroscopio, que consta de cuatro elementos: una fuente de radiación (que podrá ser una llama o un tubo de descarga), un prisma óptico (que descompone la radiación), un conjunto de lentes y un registrador (para observar el espectro obtenido y así poder identificar las radiaciones).
El fundamento de estas técnicas experimentales es el estudio de los espectros de la radiación electromagnética que emiten o absorben las sustancias al ser irradiados con una onda.
ESPECTRÓMETRO DE MASAS
La principal aplicación de la espectrometría de masas es la determinación de masas atómicas y moleculares. Se utiliza para ello el espectrómetro de masas. Este dispositivo toma una muestra de composición desconocida y la fragmenta e ioniza. Estos fragmentos cargados recorren un tubo donde existe un campo magnético, de forma que los iones describen una trayectoria curva con un radio que dependerá de la relación masa/carga (m/q) de cada ion. Los iones, ya separados, llegan a un detector y se registra así un espectro que indica masas y abundancias relativas.
En el espectrómetro de masas se distinguen tres zonas:
1. Fuente de ionización: la muestra introducida en el dispositivo es vaporizada y posteriormente ionizada por bombardeo con electrones.
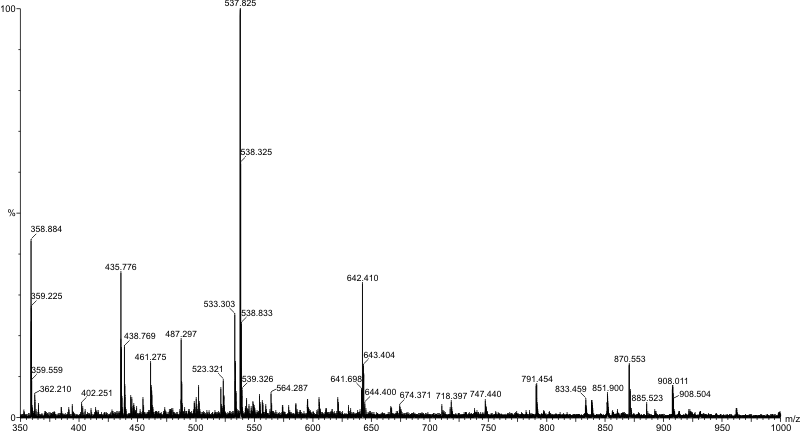 |
| Imagen de Mkotl en Wikipedia. CC |
2. El analizador de masas: los iones pasan por una región en la que un campo magnético curva las trayectorias y las separa en función de las respectivas relaciones m/q
3. El detector: este convierte el haz de iones en una señal eléctrica que posteriormente es procesada. Los resultados obtenidos son mostrados en una gráfica tal como la que se muestra en la imagen.
El siguiente vídeo te ayudará a comprender mejor el funcionamiento del espectrómetro.
Vídeo de Ernesto Brunet-Romero alojado en Youtube
Ejercicio Resuelto
Calcula la masa atómica del plomo a partir del espectro de masas de los isótopos de este elemento y su proporción isotópica.
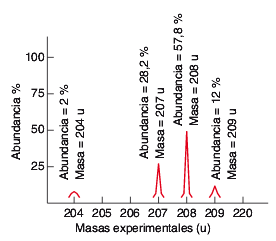
La espectrometría de masas permite, además de conocer la masa molar de una sustancia, la estructura de esta una vez que se recomponen los fragmentos obtenidos del espectrómetro. Es por ello que se utiliza para estudiar moléculas orgánicas complejas (macromoléculas, polímeros...).