3. Factores de conversión
Para evitar muchos de los errores que se cometen al realizar cálculos en las reacciones químicas, se utilizan los factores de conversión.
Un factor de conversión es una fracción que relaciona las cantidades de dos sustancias contenidas en la reacción química ajustada, o cantidades de distintas magnitudes de una misma sustancia.
El uso de los factores de conversión supone que debes establecer una secuencia de transformaciones que te facilitará la realización de los cálculos estequiométricos.
Importante
El método de factores de conversión se resume en el siguiente esquema:
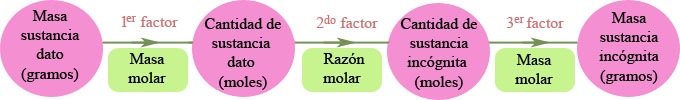
Considera el ejemplo del apartado anterior, la reacción del aluminio con el oxígeno para formar óxido de aluminio, y escribe la ecuación ajustada:
La secuencia de operaciones sucesivas es:

Y serán necesarios tres factores de conversión. Las tres etapas del cálculo quedan resumidas en una:
m(Al_2O_3)=54\: g\: de\: Al\:\cdot\:\frac{1\: mol\: de\: Al}{27 \:g\: de\: Al}\:\cdot\:\frac{2\: mol \:de\: Al_2O_3}{4\: mol\: de\: Al}\:\cdot\:\frac{102\: g\: de\: Al_2O_3}{1\: mol \:de\: Al_2O_3}= 102\: g\: de\: Al_2O_3
Para saber más
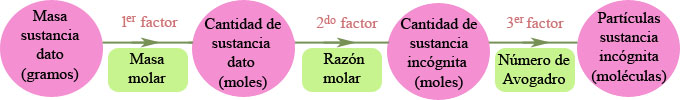
En ocasiones interesa conocer el número de partículas que se forman de una determinada sustancia en una reacción química. Para ello debes utilizar un factor, que relacione las partículas (N) con la cantidad de materia (n). Recuerda que en un mol de cualquier sustancia hay el número de Avogadro de partículas (NA).
N = n · NA
Ejercicio Resuelto
 |
| Animación de RedAndr, Creative commons |
C12H22O11 + O2 → CO2 + H2O
¿Qué masa de oxígeno consumes para quemar 10 g de azucar?
Masas atómicas relativas: H = 1; C = 12 ; O = 16
¿Cuántas moléculas de CO2 se forman en el proceso anterior?
NA = número de Avogadro = 6.02 ∙ 1023
Reflexiona
El óxido de hierro (III) se hace reaccionar con monóxido de carbono para obtener el hierro. Como producto de la reacción se forma, además, dióxido de carbono. Si dispones de 2000 kg de Fe2O3, ¿qué masa de hierro puedes obtener?
Masas atómicas relativas: C = 12 ; O = 16 ; Fe = 56