3. Formación y crecimiento de los cristales
Para saber más
 |
|
Crecimiento de cristales |
La cristalización es un fenómeno que consiste en dos procesos: la nucleación y el crecimiento cristalino.
La nucleación sería la aparición de una nueva fase (sólida) dentro de la solución. A partir de estructuras más básicas, como el agregado y el embrión, y cuando éstas alcanzan un equilibrio termodinámico con la solución, se consigue un “núcleo”. A partir de este instante pueden pasar dos cosas: que el núcleo se disuelva o que crezca dando lugar a un cristal.
 |
| Esquema del proceso de cristalización Gráfico de Jerónimo Moreno Pulido. Licencia cc |
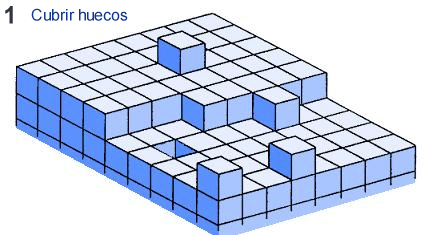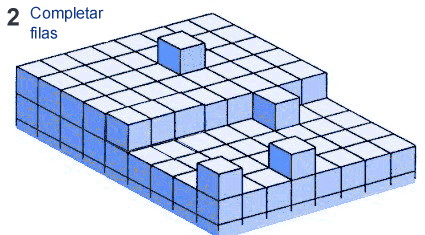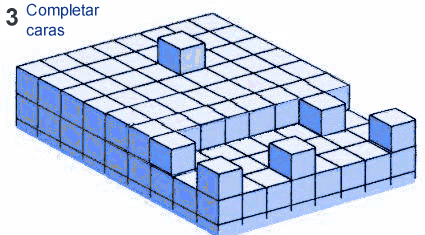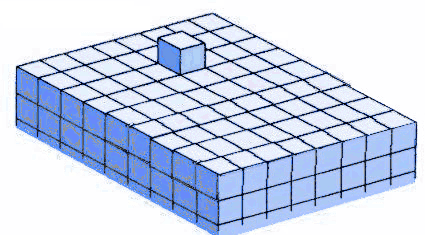
El crecimiento de un cristal depende de un conjunto de procesos por los cuales unidades de crecimiento (UC) - que pueden ser átomos, iones o moléculas - se anexionan a la superficie del mismo generando que aumente de tamaño.
En teoría, un cristal ideal crecería en equilibrio con el medio, tendría una perfecta periodicidad y simetría, y sería totalmente homogéneo e isótropo. Pero en la realidad, ese cristal no existe.
En los cristales reales se producen ciertas alteraciones internas y superficiales sobre una estructura que en teoría tendría un orden absoluto. Esas perturbaciones o defectos cristalinos no solo existen, sino que son totalmente necesarios para que el cristal se forme.
|
Cristales en crecimiento |
Las imperfecciones o defectos cristalinos son alteraciones estructurales o composicionales que tienen los cristales reales sobre el modelo periódico y homogéneo que teóricamente tendría un cristal ideal.
Pregunta de Elección Múltiple
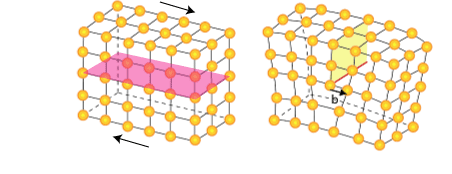 |
| Dislocación Imagen de Fredmom en Wikimedia commons. Licencia cc |
Como acabamos de comentar, los defectos cristalinos hacen referencia a cualquier perturbación en la periodicidad de la red de un cristal. Existen varios tipos. En esta página se explican brevemente cada uno de ellos.
|
Crecimiento de cristales de hielo observado con un microscopio electrónico de barrido |
Un defecto más de los cristales reales es su limitación en el espacio, por medio de caras, cuando crecen aislados libremente, o por bordes irregulares cuando crecen en agregados, acoplándose al espacio disponible entre los cristales adyacentes. Las caras de los cristales son estructuras estables, aunque los átomos que se encuentran en ellas, al tener enlaces sin saturar, son zonas con tendencia a absorber partículas, generando en ocasiones crecimiento de cristales secundarios sobre una superficie (epitaxia).
Los bordes de grano, como no se han formado libremente, no son zonas estables, y por ellas los cristales reaccionan con facilidad. A su través puede producirse el movimiento de iones entre el medio cristalino y el medio exterior, proceso frecuente en la génesis de minerales y rocas y que se llama difusión en estado sólido.
Actividad
|
Goniómetro de aplicación midiendo un ángulo diedro entre dos caras de un cristal. |
En el siglo XVIII Romé de l´Isle, siguiendo los pasos de Steno, descubrió que la composición y la forma de los cristales guardaban relación. Comprobó que dos cristales distintos de una misma sustancia, si se forman en condiciones idénticas, terminan adquiriendo formas geométricas similares porque los ángulos formados entre caras equivalentes mantienen valores constantes. Así se enunció la “Ley de la constancia de los ángulos diedros”, que supuso el inicio de la ciencia de los cristales.
Actividad
Básicamente, la cristalización de las sustancias se puede realizar por los cuatro mecanismos siguientes:
1. Condensación de un sublimado.
2. Precipitación a partir de soluciones.
3. Solidificación a partir de un fundido.
4. Transformaciones estructurales a partir de un sólido preexistente.
Actividad desplegable
Selecciona en cada caso el mecanismo mediante el cual se forman los cristales:
Objetivos
Pongamos un ejemplo.
Al aumentar la concentración en una solución de cloruro sódico los iones Na+ y Cl- tienden a unirse. En distintos puntos se van formando pequeñísimos núcleos de NaCl que tienen a su vez gran facilidad para volverse a disolver (cosa que sucede con frecuencia). Los que no se disuelven van atrayendo a otros iones Na+ y Cl- que se añaden a su superficie hasta que alcanzan un tamaño crítico, a partir del cual el crecimiento es irreversible (siempre que se mantengan las mismas condiciones de concentración).
El modo cómo se produzca la nucleación del cristal, la velocidad de crecimiento de sus caras, su forma externa o el tamaño que alcance, estarán determinados por las condiciones termodinámicas del medio de cristalización. De modo similar, los mecanismos de crecimiento están relacionados con la sobresaturación del medio y con la rugosidad de las superficies del cristal.
En este vídeo , alojado por Eric_of_le en YouTube, puedes observar cómo se van formado los cristales cúbicos de NaCl
Existen tres condiciones favorables para que se formen y crezcan bien los cristales: espacio, tiempo y reposo. Los cristales serán tanto más grandes y perfectos cuanto más espacio y tiempo hayan tenido para crecer, y menos se hayan perturbado las condiciones dinámicas del medio.
En los crecimientos rápidos (generados por enfriamiento brusco de una solución, por ejemplo) se obtienen agregados de numerosos individuos de pequeño tamaño con formas variadas (aciculares, dendríticas, etc.).
|
¿Qué son los minerales y cómo se forman? |