Resumen
Importante
Hay diferentes tipos de reacciones químicas y varias formas de clasificarlas según el criterio elegido:
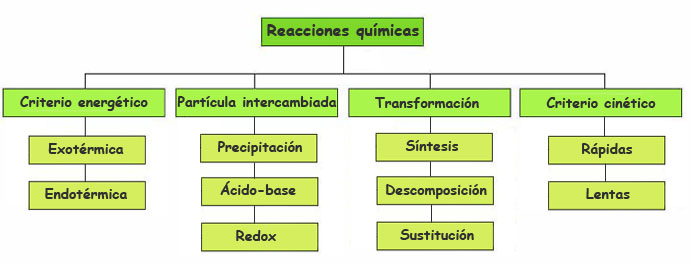
Importante
Reacciones de síntesis
Son reacciones químicas en las que dos o más sustancias (reactivos) se combinan para formar otra distinta (producto) más compleja.
La ecuación química general es:
A + B → AB
Importante
Reacciones de descomposición
Son reacciones químicas en las que un compuesto se descompone en dos o más sustancias más simples. Son las inversas de las reacciones de síntesis.
La ecuación química general es:
AB → A + B
Importante
Reacciones de sustitución o desplazamiento
Las reacciones de sustitución o desplazamiento pueden ser simples o dobles.
En una reacción de sustitución o desplazamiento simple, un elemento es reemplazado por otro elemento más reactivo en un compuesto, para producir un nuevo compuesto y el elemento desplazado.
La ecuación química general es:
A + BC → AC + B
En una reacción de doble sustitución o desplazamiento hay dos compuestos químicos que intercambian dos elementos para formar dos nuevos compuestos.
La ecuación química general es:
AB + CD → AD + CB
Importante
Si las sustancias que intervienen en la reacción no son todas gaseosas, debes utilizar la ecuación de estado de los gases ( p.V = n·R·T) para obtener el factor que en la secuencia de operaciones relacione el volumen del gas y la cantidad de sustancia:
n\:=\:\frac{P\:\cdot\:V}{R\:\cdot\:T}
Cuando las condiciones de presión y temperatura son las normales(C.N.), 273 K (0ºC) y 1 atm, puedes tener en cuenta que un mol de cualquier gas ocupa 22,4 L.