3. Alcoholes y fenoles
Curiosidad
 |
 |
|
| Metanol | Gabriel Sanz. Flickr. CC |
5 mililitros de metanol pueden matar a una persona
El 17 de noviembre de 2013,en el Festival de Cine Internacional de Ourense, fue estrenado el documental que trata este fatal suceso, con el título "METÍLICO, la bebida de la muerte" bajo la dirección de Emilio Ruiz Barrachina.
Ya sabes que cada átomo de carbono tiene que formar cuatro enlaces, por eso decimos que su valencia es 4. También sabes que la valencia del H y de los halógenos (F, Cl, Br, I) es 1, porque cada átomo de ellos forma un solo enlace. Pero ¿cuántos enlaces formará cada átomo de oxígeno? su valencia es 2 y formará dos enlaces (dos enlaces sencillos o un doble enlace).
|
Un átomo de O forma dos enlaces |
|
| -O- | =O |
Los alcoholes y los fenoles presentan el grupo funcional hidroxilo -OH (-O-H): en los alcoholes el grupo hidroxilo va unido a un carbono de un hidrocarburo (alcano, alqueno, alquino, cicloalcano, etc); es decir, el átomo de oxígeno forma un enlace simple con el hidrógeno y otro con un carbono (en los fenoles el grupo -OH irá unido a un carbono de un anillo aromático).
- Si este átomo de C está unido a un radical y a dos átomos de hidrógeno, el alcohol es un alcohol primario. Si va unido a dos radicales y a un hidrógeno, es un alcohol secundario; y si va unido a tres radicales es un alcohol terciario:
| Alcohol primario |
Alcohol secundario |
Alcohol terciario |
| R-CH2OH | R-CHOH-R´ | R-COH(R´)-R´´ |
Para nombrar los alcoholes vamos a utilizar, de forma general, la nomenclatura por sustitución. Es decir, suponemos que se ha sustituido un hidrógeno de un hidrocarburo por un grupo -OH.
- Se nombran añadiendo el localizador del grupo hidroxilo (si hace falta), entre guiones, y la terminación -ol (de alcohol), al nombre del hidrocarburo correspondiente al que se le suprime la vocal final.
| Fórmula | Nombre |
| CH3OH |
Metanol |
| CH3CH2OH | Etanol |
| CH3CHOHCH2CH2CH3 | Pentan-2-ol |
- El grupo funcional alcohol tiene preferencia respecto a los dobles y triples enlaces. Es decir, si en un compuesto nos encontramos dobles enlaces, triples enlaces y la función alcohol, nombramos primero los dobles enlaces (en, adieno, etc.), después los triples enlaces (in, diino, etc) y por último la función alcohol (-ol).
Veamos algunos ejemplos:
| Fórmula | Nombre |
| CH3CHOHCH2CH=CH2 |
Pent-4-en-2-ol |
| CH2OHCH2CH2CH2C≡CH | Hex-5-in-1-ol |
|
CH2=CHCHOHC≡CCH3
|
Hex-1-en-4-in-3-ol |
- Si en una molécula hay más de un grupo -OH utilizamos los sufijos dio, triol, tetrol, etc.
| Fórmula |
Nombre |
| CH2OHCH2OH | Etano-1,2-diol |
| CH2OHCH2CH2CH2CHOHCH2CH3 | Heptano-1,5-diol |
| CH2=CHCHOHCHOHC≡CH | Hex-1-en-5-ino-3,4-diol |
| CH(OH)2CH(CH3)CH=CHC≡CH | 2-Metilhex-3-en-5-ino-1,1-diol |
Te habrás dado cuenta de que en los ejemplos anteriores no hemos dibujado los enlaces sencillos y hemos utilizado paréntesis para indicar que en el carbono 1 del último compuesto hay dos hidróxilos (OH), y que en el carbono 2 hay un radical metil (en vez de colocarlo como una rama de la cadena principal hacia abajo o hacia arriba).
- Cuando en el compuesto hay otro grupo funcional que tiene prioridad sobre el grupo alcohol, éste se nombra como un sustituyente más, utilizando el prefijo hidroxi (de hidrógeno y oxígeno). Más adelante veremos algún ejemplo.
Importante
Importante
Curiosidad
Los alcoholes sencillos se pueden nombrar también utilizando la nomenclatura de grupo funcional. Se nombra primero el grupo funcional (alcohol) y a continuación el nombre del radical unido al grupo OH sin la -o final y terminado en -ico.
| Fórmula |
Nomenclatura por sustitución |
Nomenclatura por grupo funcional |
| CH3OH | Metanol | Alcohol metílico |
| CH3CH2OH | Etanol | Alcohol etílico |
| CH3CH2CH2OH | Propan-1-ol | Alcohol propílico |
Los fenoles son alcoholes en los que el grupo hidroxilo (-OH) va unido a un carbono de un anillo aromático. Reciben su nombre de fenol que es el más sencillo de estos compuestos.
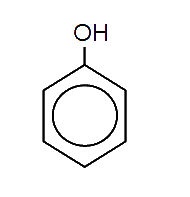 |
| Fenol |
Vamos a aprender a nombrar solo derivados del fenol:
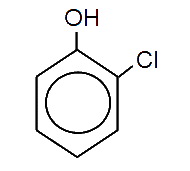
- Para nombrar los derivados del fenol se numera el anillo, empezando por el C al que va unido el grupo OH, de manera que la combinación de localizadores que le corresponde a los sustituyentes sea la más baja posible. Si sólo hay un sustituyente podemos utilizar los términos o- (orto), m- (meta) y p- (para) en lugar de los localizadores 2, 3 o 4:
 |
 |
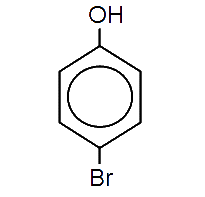 |
| o-Clorofenol | m-Fluorofenol | p-Bromofenol |
AV - Actividad de Espacios en Blanco
AV - Reflexión
1. Propan-1-ol
2. Pentan-2-ol
3. Hex-4-en-2-ol
4. Fenol
5. But-3-in-1-ol
Importante
En los compuestos polifuncionales en los que el alcohol no interviene como función principal, se designa con el prefijo hidroxi-.
Propiedades físicas de los alcoholes
son solubles en agua, debido a la polaridad del grupo hidroxilo (OH).
Algunos usos y aplicaciones:
- barnices (metanol)
- combustible (etanol)
- jabón de glicerina (propano-1,2,3-triol)
- anticongelante (etano-1,2-diol)
cuando los dos átomos unidos por enlace covalente tienen electronegatividad diferente la hay una distribución no homogénea de la nube de carga, formándose un dipolo
Curiosidad
 |
| Imagen de elaboración propia |
 |
|
Antiguo alambique Imagen de elaboración propia |
 |
| Etanol |