2.5 Derivados halogenados de los hidrocarburos
Pre-conocimiento
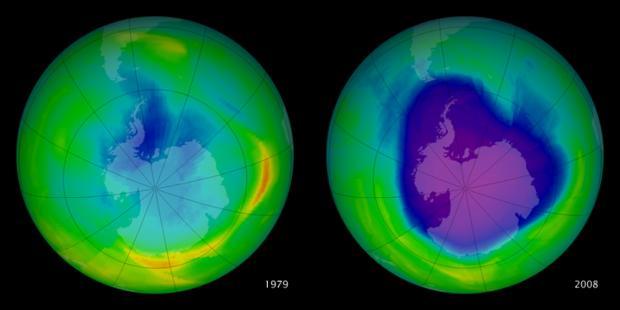 |
| Agujero en la capa de ozono en 1979 y en 2008. NASA |
 |
|
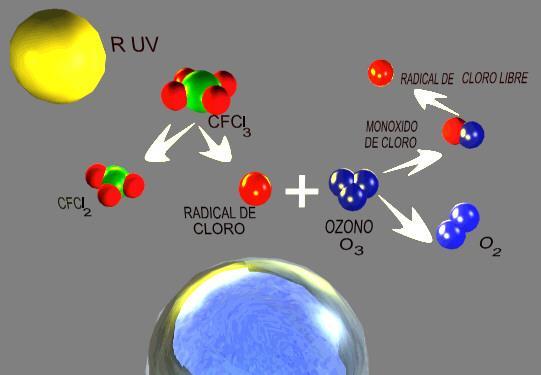
Destrucción del ozono por los CFCs. J.A. Pérez Leal. Wikipedia |
En este apartado vas a aprender a formular derivados halogenados de los hidrocarburos, es decir, compuestos que se obtienen cuando se sustituyen hidrógenos de un hidrocarburo por átomos de fluor (F), cloro (Cl), bromo (Br) o yodo (I).
Los clorofluorocarbonos (CFCs) que, como hemos visto, son los responsables del agujero en la capa de ozono son derivados halogenados de los hidrocarburos que se obtienen al sustituir algunos o todos los hidrógenos de un hidrocarburo por cloro y fluor.
Los halogenos (F, Cl, Br, I) tienen 7 electrones en su último nivel por lo que necesitan un electrón más para ser estables como el gas noble que le sigue en su periódo. Para ello comparte uno de estos 7 electrones con otro átomo que aportará también un electrón al enlace covalente que se forma. Por tanto, cada átomo de F, Cl, Br o I forma un único enlace covalente cuando se une a un átomo de C al sustituir a un átomo de H en un hidrocarburo.
- Los átomos de F, Cl, Br o I sustituidos se indican delante del nombre del hidrocarburo utilizando los prefijos fluoro-, cloro-, bromo-, o yodo- con los prefijos multiplicativos que indican su número (di-,tri-,tetra-,etc) y los localizadores correspondientes si hacen falta. Si hay más de un halógeno en una molécula se nombran por orden alfabético.
Vamos a empezar viendo algunos ejemplos de CFCs:
| Ejemplos de CFCs | |
| CCl3F | Triclorofluorometano |
| CCl2F2 | Diclorodifluorometano |
| CClF=CF2 |
Clorotrifluoroeteno |
| CCl2F-CCl2F | 1,1,2,2-Tetracloro-1,2-difluoroetano |
Otros ejemplos de derivados halogenados de los hidrocarburos son:
| Fórmula | Nombre |
| CHCl3 | Triclorometano |
| CH3-CHCl-CH3 | 2-Cloropropano |
| CH2=CH-CH2Br | 3-bromoprop-1-eno |
|
CHI2-C≡C-CH3
|
1,1-Diyodopropino |
| CHF=CH-CH=CH2 | 1-Fluorobuta-1,3-dieno |
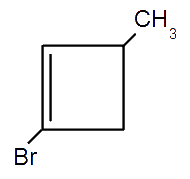 |
1-Bromo-3-metilciclobuteno |
Vamos a comentar algunas cosas de los ejemplos anteriores:
- Como curiosidad decirte que el CHCl3 se conoce con el nombre común de cloroformo. Seguro que has visto alguna película donde lo han utilizado para dormir a alguien.
- En el CH2=CH-CH2Br hemos numerado los carbonos dándole preferencia al doble enlace. Los halogenos se tratan como si fueran radicales (metilo, etilo, etc). Los carbonos se numeran dando prioridad a los dobles y triples enlaces de manera que a los radicales les correspondan los localizadores que formen la combinación más baja posible.
- Si te fijas en el último compuesto CHI2-C≡C-CH3 entenderás mejor lo de antes. Si numeramos los carbonos de izquierda a derecha los dos átomos de I van en el carbono 1 y el doble enlace en el carbono 2. Si numeramos al revés, de derecha a izquierda, el doble enlace sigue yendo en el carbono 2 pero los átomos de yodo iran en el carbono 3. Como al doble enlace le corresponde el mismo localizador de las dos maneras, elegimos aquella en la que el localizador del yodo sea más pequeño. Además, al nombrar este compuesto no hemos indicado la posición del triple enlace porque sólo hay una posibilidad. No puede ir en el carbono 1 porque éste está unido a dos átomos de I.
Importante
- Los átomos de F, Cl, Br o I se tratan como si fueran radicales (metil, etil, etc) a la hora de elegir la manera de númerar los carbonos de la cadena principal o del ciclo.
- Utilizaremos los prefijos fluoro-, bromo-, cloro-, o yodo- con los localizadores (si hacen falta) y los prefijos multiplicadores (di-, tri-, etc) delante del nombre del hidrocarburo correspondiente que se nombrará como ya hemos visto según sea un alcano, alqueno, alquino, etc.

AV - Actividad de Espacios en Blanco
AV - Reflexión
Formula los siguientes compuestos:
1. 1,2-Dicloropropano
2. Flurorotriclorometano
3. o-Cloroetilbenceno
4. 1,2-Difluoropropeno
5. 4-Bromociclopenteno