1.1 Ejemplos de cambios físicos
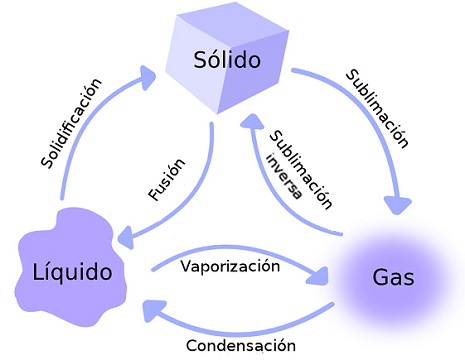 |
| Adaptado de Imagen en Wikimedia commons de Josell7. Licencia GNU Free |
Cuando calentamos agua hasta que hierve, como hizo Belén para prepararse el té, el agua experimenta un cambio de estado, pasando de líquido a sólido.
Vamos a estudiar dos tipos de cambios físicos:
1. Cambios de estado.
2. Mezclas.
Empecemos con los primeros.
Los cambios de estado físico se producen, fundamentalmente por absorción o desprendimiento de energía. Así, si calentamos agua hasta llegar a los 100ºC, ésta pasa de estado líquido a vapor. Por el contrario, si disminuimos su temperatura hasta 0ºC, el agua líquida pasará a estado sólido y tendremos hielo. Lo mismo sucede con otras sustancias, aunque los puntos de ebullición y de fusión varían para cada una.
A veces se oye decir: el vapor, con el frío, se hizo agua. Es incorrecto. Tanto el vapor de agua como el agua líquida son la misma sustancia: agua. La condensación del vapor es tan solo un cambio físico de estado gaseoso a líquido.
En este ![]() vídeo de la Eduteca puedes aprender más sobre cambios de estado del agua.
vídeo de la Eduteca puedes aprender más sobre cambios de estado del agua.
Curiosidad
 |
| Imagen en Pixabay de Frank Winkler. Dominio público |
La temperatura es responsable de otros tipos de cambios físicos.
¿Te has dado cuenta de que durante el verano cuesta más ponerse o quitarse los anillos? Eso es debido a que con el calor los dedos se dilatan, se hacen algo más anchos y por eso el anillo entra más ajustado. En invierno sucede lo contrario.
Al bajar la temperatura los dedos se contraen un poco, y es más fácil colocárselos. Contracción y dilatación son también cambios físicos.
Así que, para no tener problemas durante el intercambio de anillos, es mejor casarse en invierno que en verano, o tener a mano unos cubitos de hielo, por si hay que enfriarle el dedo a uno de los novios. ![]()
Pasemos ahora a las mezclas.
¿Recuerdas cuando Belén echó azúcar al té?
En realidad, lo que estaba haciendo era juntar varias sustancias pero sin que reaccionaran químicamente. Elaboró una mezcla homogénea o disolución.
¿Por qué las disoluciones son homogéneas? Pues porque no podemos distinguir sus componentes a simple vista. Una vez que se juntan, no eres capaz de distinguir el azúcar del té.
Si dejas pasar un tiempo, el líquido se evaporará y el azúcar se quedará depositado en el fondo de la taza. Esto no sucedería si hubiera habido un cambio químico. No sería tan fácil volver atrás.
 |
 |
 |
| Niebla | Vino | Acero |
| Imagen en Pixabay de blickpixel. Dominio público | Imagen en Pixabay de Didgeman. Dominio público | Imagen en Pixabay de hpgruesen. Dominio público |
Importante
Una disolución es una mezcla homogénea de varias sustancias. A las sustancias que forman una disolución se les llama componentes.
- Al componente que se encuentra en mayor proporción se le denomina disolvente y determina el estado de la disolución (sólido, líquido y gaseoso).
- Al que se encuentra en menor cantidad se le denomina soluto.
Para saber más
¿Cuántos tipos de disoluciones hay?
Pues tenemos nueve combinaciones, dependiendo de en qué estado se encuentren el disolvente y el soluto:
| Disolvente | Soluto | Ejemplos |
| Sólido | Sólido | Aleaciones de metales:acero (hierro y carbono) |
| Líquido | Amalgamas (mercurio + metal) | |
| Gas | Carbono activo y los gases absorbidos por él. | |
| Líquido | Sólido | Agua del mar, agua y azúcar |
| Líquido |
agua y alcohol | |
| Gas |
Bebidas con gas, espuma de afeitar | |
| Gas | Sólido | Humo |
| Líquido |
Niebla, aerosoles | |
| Gas | Aire |
Curiosidad
¿Sabías que son muy distintas cuando se disuelven?
 |
| Imagen en Pixabay de Fotomek. Dominio público |
No todas las sustancias se comportan de la misma manera en el agua, por ejemplo la sal y el azúcar, cuando las disolvemos en agua, aparentemente son iguales, podríamos confundirlas, sino fuera por su sabor distinto, sin embargo, son moléculas distintas, que en el agua de comportan de distinta forma. Si lo quieres ver, pincha en las siguientes animaciones del Proyecto TIGER de CNSSM con Licencia cc:
Has visto que la sal en agua conduce la electricidad, por eso se dice que es un electrolito, porque en disolución se separa la molécula en sus iones (átomos con carga recuerdas), mientras que el azúcar no es un electrolito, no se separan sus átomos en agua (no se forman iones) por lo que no conducen la electricidad.
Para saber más
En este vídeo puedes aprender más cosas interesantes sobre las disoluciones y su importancia en la vida cotidiana.
Video de traful en Youtube
Pregunta Verdadero-Falso
Indica si las siguientes afirmaciones son verdaderas o falsas
Retroalimentación
Falso
Hay disoluciones en las que sucede al revés, por ejemplo en las amalgamas.
Retroalimentación
Falso
No, la fusión es el paso de sólido a líquido y la condensación de gas a líquido.
Retroalimentación
Verdadero
Recuerda que el paso de gas a sólido se denomina sublimación inversa.
Retroalimentación
Falso
Las dilataciones y contracciones son cambios de forma debidos a variaciones de la temperatura.