3. Modelo atómico de Thomson
La primera de estas partículas en descubrirse fue el electrón, identificado por J.J. Thomson a partir de los resultados obtenidos en la experimentación de gases a baja presión en un dispositivo denominado tubo de rayos catódicos, que puedes observar a continuación:
| Grabación de animación de Mariano Gaite Cuesta |
Ahora bien, al aplicar un campo eléctrico sobre la trayectoria de los rayos se observó que estos se desviaban hacia la placa cargada positivamente, lo que indicaba claramente que dicha radiación estaba cargada, y más concretamente formada por partículas de carga negativa.
 |
| Imagen en Wikipedia. CC |
Tras el estudio detallado de estas desviaciones, se encontró que se trataba de partículas cargadas negativamente y fácilmente desviables (de poca masa). Se pudieron describir las características de un diminuto electrón.
|
Propiedades me = 9,1 10-31 kg qe = - 1,6 10-19 C |
Se encontró que el electrón era una partícula con una masa extremadamente pequeña, exactamente 9,1 10-31 kg. También se encontró que el electrón tenía una carga eléctrica negativa, con un valor de 1,6 10-19 C.
El culombio (C) es la unidad de carga eléctrica en el Sistema Internacional de Unidades y se corresponde con la carga de 6,24 × 1018 electrones.
Actividad
El electrón es una partícula constituyente del átomo, caracterizada por:
- Carga eléctrica negativa.
- Masa extremadamente pequeña.
AV - Reflexión
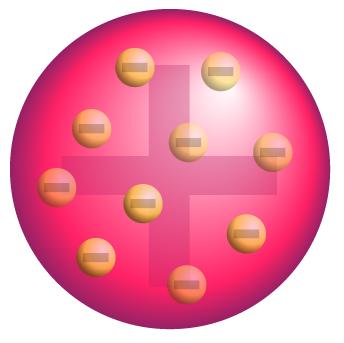 |
| Imagen en Wikipedia. Dominio público |
Actividad
Actividad de Espacios en Blanco
La siguiente frase describe el átomo propuesto por Thomson, escribe las palabras que faltan.