Descripción de la tarea

1. Define el concepto de velocidad de reacción e indica las unidades en las que generalmente se suele expresar.
2. En la reacción A + 3 B → 2 C, en un determinado momento, el reactivo B está reaccionando a la velocidad de 0,18 M/s1. Contesta a las siguientes cuestiones:
- ¿A qué velocidad desaparece el reactivo A?
- ¿Con qué velocidad aparece el producto C?
3. Para la reacción A + B → 2C, se ha comprobado experimentalmente que es de primer orden respecto al reactivo A y de segundo orden respecto al reactivo B.
- Escribe la ecuación de velocidad.
- ¿Cuál es el orden total de la reacción?
- Determina las unidades de la constante k
4. Justifica razonadamente si las siguientes afirmaciones son verdaderas o falsas:
- La velocidad de una reacción aumenta al disminuir la temperatura a la que se realiza.
- La velocidad de una reacción aumenta al aumentar la energía de activación.
- La velocidad de una reacción disminuye al disminuir la concentración de los reactivos.
- La velocidad de la reacción no depende de la temperatura.
- La acción de un catalizador no influye en la velocidad de reacción.
5. A la luz de la siguiente gráfica, responde:
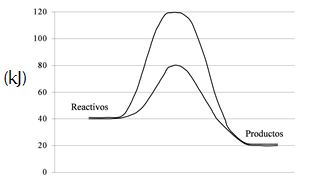
- ¿Cuánto vale Ea?
- Explica el efecto que produce un aumento de la temperatura en la velocidad de la reacción.
6. En el laboratorio se llevan a cabo tres ensayos para determinar experimentalmente la ecuación de velocidad de A + B → C. Los resultados se anotan en la siguiente tabla:
|
Experiencia |
[A] (mol·L-1) |
[B] (mol·L-1L) |
v (mol·L-1·s-1) |
|
1 |
0.25 |
0.25 |
3.71 |
|
2 |
0.50 |
0.25 |
7.42 |
|
3 |
0.25 |
0.50 |
14.84 |
Determina tanto los órdenes de reacción total y parciales, como el valor de k y sus unidades.
7. [Prueba septiembre 2019] Indica si las siguientes afirmaciones son verdaderas (V) o falsas (F) y justifica tus respuestas:
[ ] La velocidad de una reacción química aumenta proporcionalmente a la cantidad de catalizador que
añadimos a la vasija de reacción.
[ ] Los únicos factores que influyen en la velocidad de una reacción son el estado de agregación de los
reactivos y la temperatura.

A la hora de resolver la tarea, debes elaborar un documento con el resultado de la tarea y enviárselo a tu profesor/a. Puedes utilizar esta plantilla para su desarrollo, aunque también puedes elaborar tu propia plantilla. Si haces esto último, debes indicar el enunciado de cada uno de los apartados previo a su resolución. Recuerda, al guardar la plantilla en tu ordenador, cambiar el nombre al documento incluyendo tu nombre y apellidos siguiendo este modelo apellido1_apellido2_nombre_PACQU_U3_T3.
Si quieres elaborar esquemas o dibujos, puedes hacerlos manualmente, escanearlos e insertarlos en el documento de texto.